Ez a weboldal sütiket használ
A jobb szolgáltatás nyújtásának érdekében sütiket használunk. Az oldal jobb felhasználása érdekében kérjük, fogadja el a sütiket. További információ itt: Adatvédelmi tájékoztató
2022-04-13 15:07:15
Prof. Dr. Helyes Zsuzsanna orvos, neurofarmakológus, a Pécsi Tudományegyetem Általános Orvostudományi Kar Farmakológiai és Farmakoterápiai Intézetének egyetemi tanára, a Szentágothai János Kutatóközpont elnöke, a Magyar Tudományos Akadémia Orvosi Osztályának tagja, számos díj, elismerés, köztük a Mestertanár Aranyérem birtokosa, bel- és külföldi szakmai társaságok tagja. Az Erdélyi Múzeum Egyesület Orvos- és Gyógyszerésztudományi Szakosztálya 30. közgyűlésének plenáris előadójaként tartott hosszú tapssal jutalmazott, érdekfeszítő előadást.
„A pécsi neurofarmakológus professzor kutatási területe a kapszaicinérzékeny érzőidegek és neuropeptidek vizsgálata légúti, ízületi és bőrgyulladásban, fájdalomfolyamatokban, továbbá új szerkezetű gyulladásgátló és fájdalomcsillapító gyógyszerek fejlesztése.”
– Mikor választotta ezt a kutatási területet? Már egyetemi hallgatóként is vonzotta ez a rendkívül aktuális téma? Előadásában is elhangzott, a manapság használatos opioid és nem szteroid szerkezetű fájdalomcsillapítóknak, gyulladáscsökkentő szereknek számos kellemetlen mellékhatása van.
– Diákkörösként az Anatómiai Intézetben kutattam, neuroendokrin témában dolgoztam. Mindig is vonzott a kutatás, bár eredetileg klinikusnak, gyermekgyógyásznak vagy belgyógyásznak készültem.
1995-ben végeztem az orvosi egyetemet, és tősgyökeres pécsiként szülővárosomban szerettem volna maradni, de az említett területeken nem sikerült klinikai állást kapnom. PhD-hallgatóként kezdtem el dolgozni 1995 szeptemberében a Farmakológiai és Farmakoterápiai Intézetben, amit akkoriban átmeneti állapotnak tekintettem. Arra gondoltam, hogy klinikai munkámat megalapozza a kutatás, de akkori főnököm, intézetvezetőm, Szolcsányi János professzor, akadémikus olyan szinten „megfertőzött” a szenzoros idegrendszer kutatásának a szeretetével és a fájdalom-gyulladás farmakológiájának izgalmas, érdekes területével, hogy végül ott maradtam. A tudományos doktori fokozat, a PhD megvédése, a szakvizsgáim letétele következett, majd egy és utána két pályázat, aztán egy hallgató, kettő, a csoport bővült, és az irány, amelyen elindultam, visszafordíthatatlanná vált. Ma már egy percig sem bánom, hogy így alakult.

Prof. Dr. Helyes Zsuzsanna
Fotó: Bodolai Gyöngyi
– Ilyen sokat ígérő eredmények birtokában hogyan lehetne akármit is bánni? Már közhelynek hangzik, hogy a fájdalom egyidős az emberiséggel, de ez a valóság. Előadásában részletesen beszélt, jól szerkesztett táblázatokat mutatott a fájdalom eredetéről, típusairól. Az évszázadok során hogyan tekintettek a fájdalomra?
– A tartós fájdalom mindig megkeserítette az emberek életét. Az akut fájdalom egy elhárító, védekező reakciót indít be, ami jó, mert arra figyelmeztet, hogy valamit tenni kell a károsító tényező ellen, egy gyulladt fog esetében például csökkenteni kell a gyulladást. Amikor érezzük, hogy forró egy kályha, el kell húznunk a kezünket, ezért is mondhatjuk, hogy a heveny fájdalom hasznos. Azoknak az embereknek a helyzete, akiknek a fájdalomérzete valamilyen genetikai vagy egyéb betegség hatására nem megfelelő, nagyon nagy gondot jelent.
– Egyik oldalon vannak ők, a másikon azok, akik éveken, akár egy életen át sem szűnő fájdalomtól szenvednek.
– A krónikus fájdalom egészen más, az életminőséget és a munkaképességet nagymértékben csökkenti, óriási egészségügyi és társadalmi probléma. Hátterében gyakran nincs semmi azonosítható ok, amelyet kezelni lehetne. A tartós idegi károsodás komponenseket is tartalmazó (neuropátiás) fájdalomállapotok igazi terápiás kihívást jelentenek. Sajnos a mechanizmus szempontjából ma sincs a kezünkben több fájdalomcsillapító lehetőség, mint több száz évvel ezelőtt, ezért fontos e terület kutatása.
– Melyek a klasszikus fájdalomcsillapítók „problémái”, mellékhatásai?
– A jelenlegi fájdalomcsillapítók két fő hatásmechanizmuson keresztül hatnak. Az egyik a morfinszerű, kábító fájdalomcsillapítás opioid vegyületekkel, amelyekre összetett, központi és perifériás idegrendszeri támadáspont jellemző. Az opioid receptor aktiváció egyrészt a perifériáról a központi idegrendszer felé a fájdalominger továbbítását gátolja, másrészt a leszálló fájdalomgátló pályarendszert aktiválja. Sokféle ilyen erős, kábító fájdalomcsillapító van, ami az idegi fájdalmak egy részére hat, de jelentős részére sajnos nem. Hónapokon át történő alkalmazásuk számos problémával, mellékhatással jár, mint pl. a hozzászokás, függőség, székrekedés, légzésdepresszió.
A másik gyógyszercsoport az aszpirin mintájára működő nem szteroid gyulladáscsökkentők, fájdalom- és lázcsillapítók, amelyek a fájdalom-, és gyulladáskeltő prosztaglandinok termeléséért felelős ciklooxigenáz enzimet gátolják. Közepes vagy enyhe hatásúak, fejfájás, zsigeri fájdalom, gyulladásos fájdalom csillapítására alkalmasak, de a hosszan tartó, krónikus idegi eredetű fájdalomra egyáltalán nem hatnak. Mellékhatás-spektrumuk szintén nagyon széles, pl. a jól ismert gyomor-bél rendszeri károsítás, vesekárosítás, trombotikus szövődmények és szív-ér rendszeri problémák.
E két csoporton kívül szóba jönnek bizonyos epilepszia és depresszió kezelésére használt, központi idegrendszeren ható gyógyszerek (adjuváns analgetikumok), de egyéb lehetőség nem áll rendelkezésünkre.
– Ezek szerint a kutatások olyan új fájdalomcsillapítók fejlesztésére irányulnak, amelyek hatásosan csökkentik a tartós, idegi eredetű fájdalmat, és nincsenek vagy nagyon enyhe mellékhatásaik vannak.
– Elsősorban idegi eredetű krónikus fájdalom kezelésére fókuszálunk, mint pl. a perifériás idegrendszer különféle károsodása, cukorbetegség, tumorellenes gyógyszerek, trauma, baleset vagy műtét, degeneratív vagy gyulladásos ízületi károsodás következtében kialakuló állapotok. Primér krónikus fájdalomállapot a fibromyalgia, amelyben nincs gyulladásos mechanizmus, a betegnek mégis széles körű izomrendszeri fájdalma van. Valószínűleg stresszfaktorok és a depresszió is szerepet játszanak a mechanizmusában, azonban a kialakításában szerepet játszó tényezők nem ismertek. A krónikus primér fájdalomállapotokhoz sorolható a krónikus regionális fájdalom szindróma, amelynek autoimmun tényezője is lehet. Ezek a tartós tünetek, amelyek ellenállnak minden jelenlegi fájdalomcsillapítónak, óriási problémát jelentenek a betegeknek éveken, évtizedeken át.
– A csípős paprikában lévő kapszaicinnek az érzőideg-végződésekre gyakorolt hatását évek óta kutatják a pécsi egyetemen, az utóbbi időben milyen eredményre jutottak?
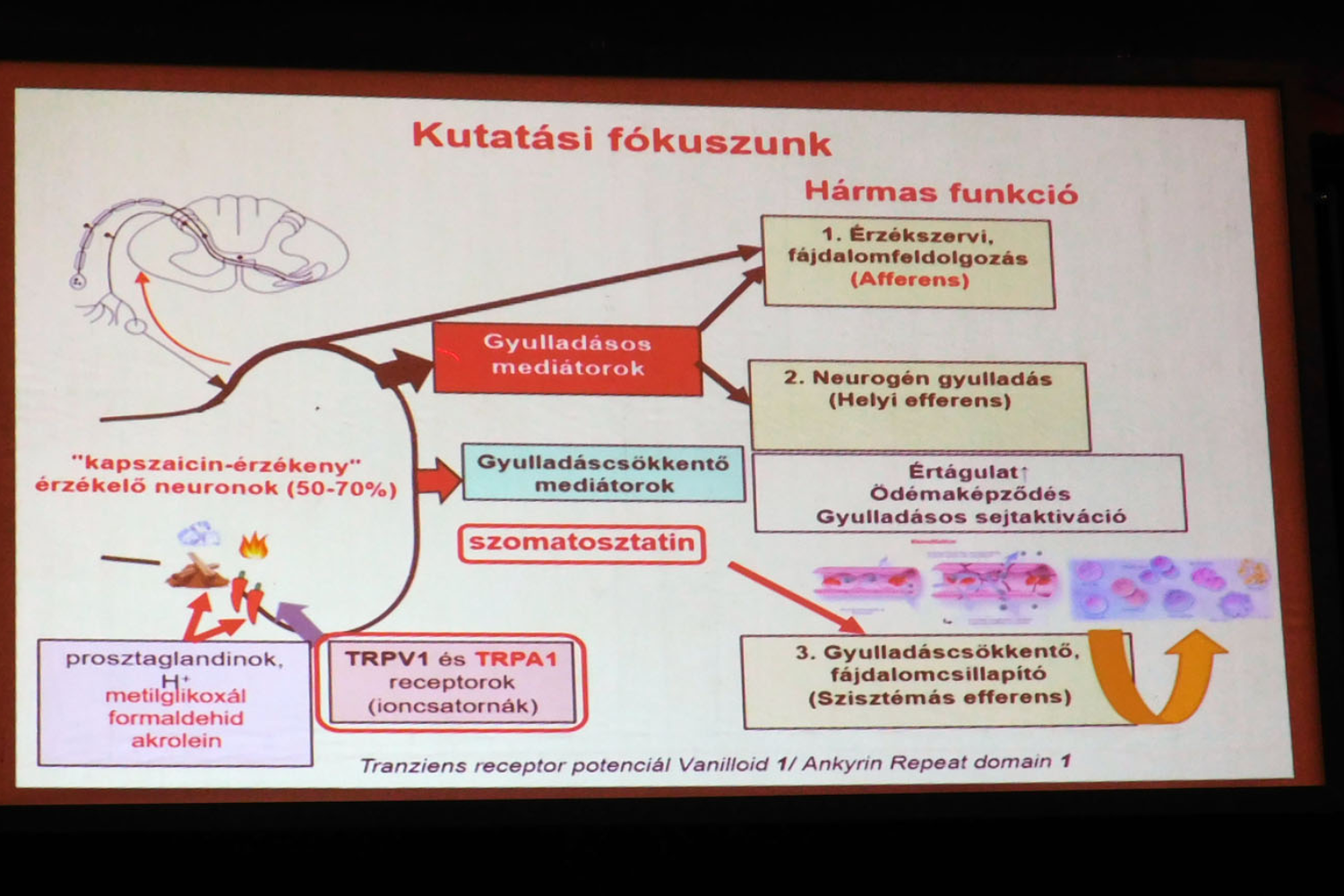
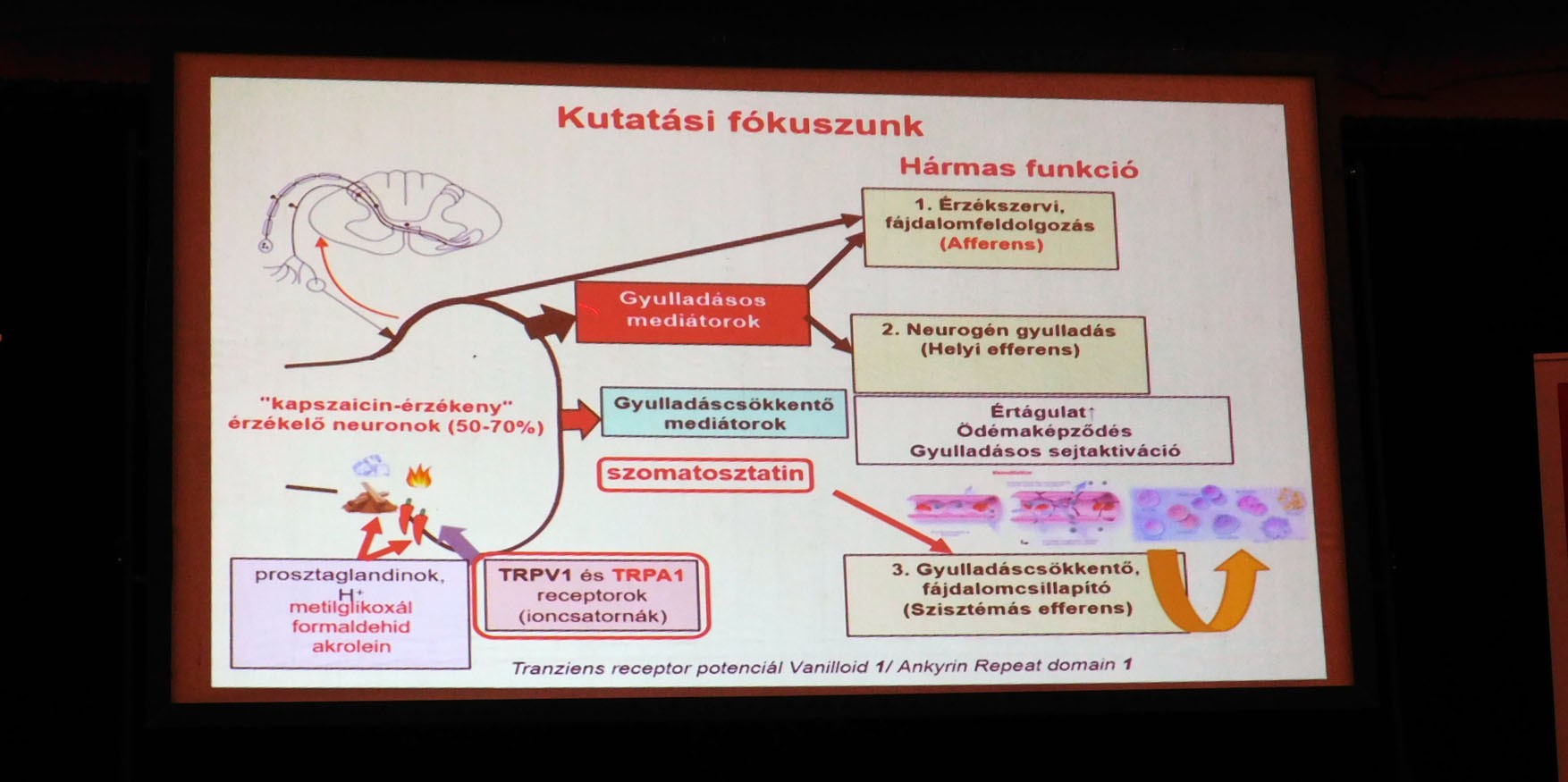
– A kapszaicin hatásainak és hatásmechanizmusának kutatására irányuló témát Szolcsányi János professzor úr hozta magával Szegedről, amikor Pécsre jött. Nagyon szerencsésnek mondhatom magam, mert az ő egyik tanítványa lehettem, ő volt a mesterünk. A kapszaicin célmolekulájára (Tranziens Receptor Potenciál Vanilloid 1: TRPV1 ioncsatorna) ható (elsősorban gátló) fájdalomcsillapító gyógyszerek fejlesztésével világszerte számos gyógyszergyár foglalkozott. 1997-ben sikerült ezt a receptort azonosítani, klónozni, felfedezésért a kaliforniai David Julius professzor 2021-ben az egyik orvosi Nobel-díjat kapta.
Bár a 2000-es években intenzíven fejlesztett TRPV1-blokkoló fájdalomcsillapító-jelöltek nagyon hatékonyak voltak, a fő problémát a hipertermizáló (testhőmérsékletet kórosan emelő) mellékhatásuk jelentette, mivel e receptor a hőszabályozásban is fontos szerepet játszik. Több értékes gyógyszerjelölt e mellékhatás miatti bukása ellenére ez az irány még nem teljesen reménytelen, mert a receptor aktivációs mechanizmusainak a mélyebb kutatása egyértelművé tette, hogy vannak olyan TRPV1-gátlók, amelyek nem hipertermizálnak.
Időközben a TRP receptorcsalád nagyon hasonló TRPA1 ioncsatorna tagjára irányuló kutatások egyre jobban előtérbe kerültek. A TRPA1 ugyancsak fontos szerepet játszik krónikus fájdalomban, azonban a hőszabályozásban nem vesz részt. A mi munkánk arra is irányul, hogy ezekre az ioncsatornákra hogyan tudunk hatni, aktivációjukat hogyan tudjuk közvetlenül vagy közvetettem gátolni a természetes, endogén aktivátorok képződésének gátlásával. A pécsi kutatások egyik vonala a Semmelweis Egyetemmel és Mátyus Péter gyógyszerkémikus professzorral együttműködve erre irányul. Nagy reményeink vannak a jelenleg fázis 1 klinikai vizsgálatok alatt álló gyógyszerjelöltünkre vonatkozóan. Az elmúlt 10 évben elvégzett, állatkísérleteket is magukba foglaló preklinikai vizsgálatok sikeresek voltak, az Országos Gyógyszerészeti és Élelmezés-egészségügyi Intézettől megkaptuk a fázis 1 klinikai vizsgálatra vonatkozó hatósági engedélyt egészséges önkéntesen végzett tolerálhatósági vizsgálatokra, amelyet reményeink szerint idén év végére befejezünk. Utána kezdődhet a krónikus fájdalomállapotokban szenvedő betegcsoportokon való tesztelés.
– Mennyi idő van még hátra, amíg ebből a hatóanyagból forgalomba kerülő gyógyszer lehet?
– Legkevesebb 5-6 év.
– Említette a professzor asszony, hogy egy bécsi céggel fognak együttműködni.
– Egy Bécsben működő kis cég, az Algonist GmbH – amit közösen hoztunk létre ott élő magyar és külföldi, valamint hazai kollégákkal – az új fájdalomcsillapító-jelöltünk klinikai vizsgálatára és további új molekulák azonosítására, optimalizálására fog összpontosítani, egyetemünkkel szoros együttműködésben.
– További sikeres kutatómunkát kívánok!
Szemléletváltásra van szükség



















